La terapia sostitutiva con gli analoghi dell’insulina è indicata nella cura sia
-del diabete mellito tipo 1, d’origine autoimmunitaria, ove la secrezione d’insulina da parte del pancreas manca completamente; sia
-del diabete mellito tipo 2 avanzato (generalmente dopo fallimento delle altre terapie), ove la produzione d’insulina da parte del pancreas è insufficiente rispetto alle necessità, anche a causa di una notevole resistenza periferica alla sua azione (insulino-resistenza).
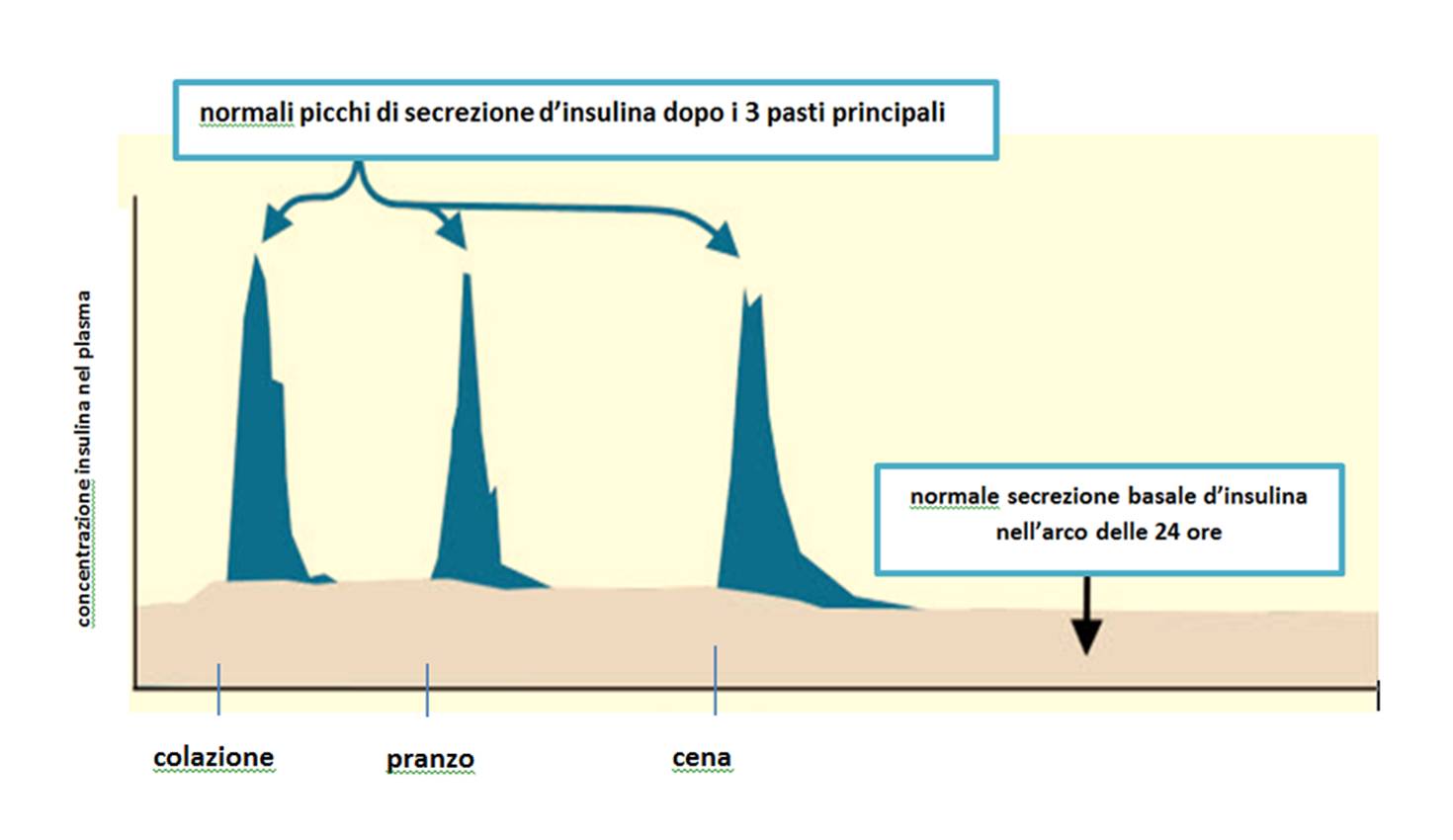
L’attività farmacologica principale dell’insulina si esplica sulla capacità di ridurre la glicemia (effetto ipoglicemizzante). Si usano in terapia gli analoghi rapidi dell’insulina umana (lispro, aspart, glulisina) e gli analoghi lenti (glargine e detemir). Il trattamento insulinico sostitutivo viene impostato in modo tale da ricalcare la secrezione normale d’insulina da parte delle cellule del pancreas (le beta-cellule delle insule pancreatiche), ossia una lieve secrezione continua e costante d’insulina (cosiddetta secrezione basale) nell’arco delle 24 ore e picchi di secrezione ormonale in corrispondenza dei pasti (fig. 1).
Fig. 1- secrezione normale dell’insulina
L’analogo rapido insulinico viene somministrato sottocute in boli subito prima dell’inizio di ogni pasto (compresi gli spuntini). Questo tipo di somministrazione vuole imitare la fisiologica reazione del pancreas normale in seguito all’aumento della glicemia dopo un pasto: si verifica una liberazione consistente d’insulina, in grado di riportare alla norma l’iperglicemia post-prandiale (fig. 2).
Entro le quattro ore successive alla somministrazione l’analogo insulinico rapido riduce la glicemia in quanto favorisce l’ingresso del glucosio in quasi tutte le cellule dell’organismo (tranne quelle del sistema nervoso che sono liberamente permeabili all’ingresso del glucosio). Il glucosio è il combustibile utilizzato da tutte le cellule per produrre energia sotto forma di ATP. Nelle cellule del fegato e dei muscoli il glucosio sotto l’influenza dell’insulina viene trasformato in glicogeno, che è un composto energetico di riserva.
Tuttavia il pasto non apporta all’organismo solo carboidrati (da cui deriva il glucosio), ma anche altri nutrienti, tra cui grassi e proteine, dalla cui digestione intestinale provengono rispettivamente gli acidi grassi e gli aminoacidi. Le azioni secondarie dell’analogo insulinico si esercitano –proprio come fa l’insulina nativa- anche sugli acidi grassi e gli aminoacidi. I primi tramite il circolo linfatico raggiungono la circolazione sanguigna, prima, e il tessuto grasso (adiposo), poi. Qui per effetto dell’insulina vengono captati dalle cellule adipose e trasformate in trigliceridi (altro materiale energetico di riserva). Gli aminoacidi invece, per azione dell’insulina, sono captati soprattutto dai muscoli e dal fegato, ove vengono trasformati in proteine. In definitiva gli effetti metabolici secondari dell’insulina consistono nell’accumulo di scorte energetiche sotto forma di glicogeno, grassi e proteine.
L’analogo lento dell’insulina (o insulina basale,) viene iniettato sottocute una volta al giorno, in genere la sera tardi prima di andare a letto (fig. 2); esso è assorbito molto lentamente dal sito d’inoculo per cui la sua durata d’azione è di circa 24 ore. L’analogo basale svolge un ruolo metabolico importante nel periodo post-assorbitivo, che comprende il periodo del digiuno notturno e i periodi di digiuno interprandiali (dalla quarta ora dopo un pasto al pasto successivo).
Fig. 2 – profilo insulinemico dopo somministrazione degli analoghi
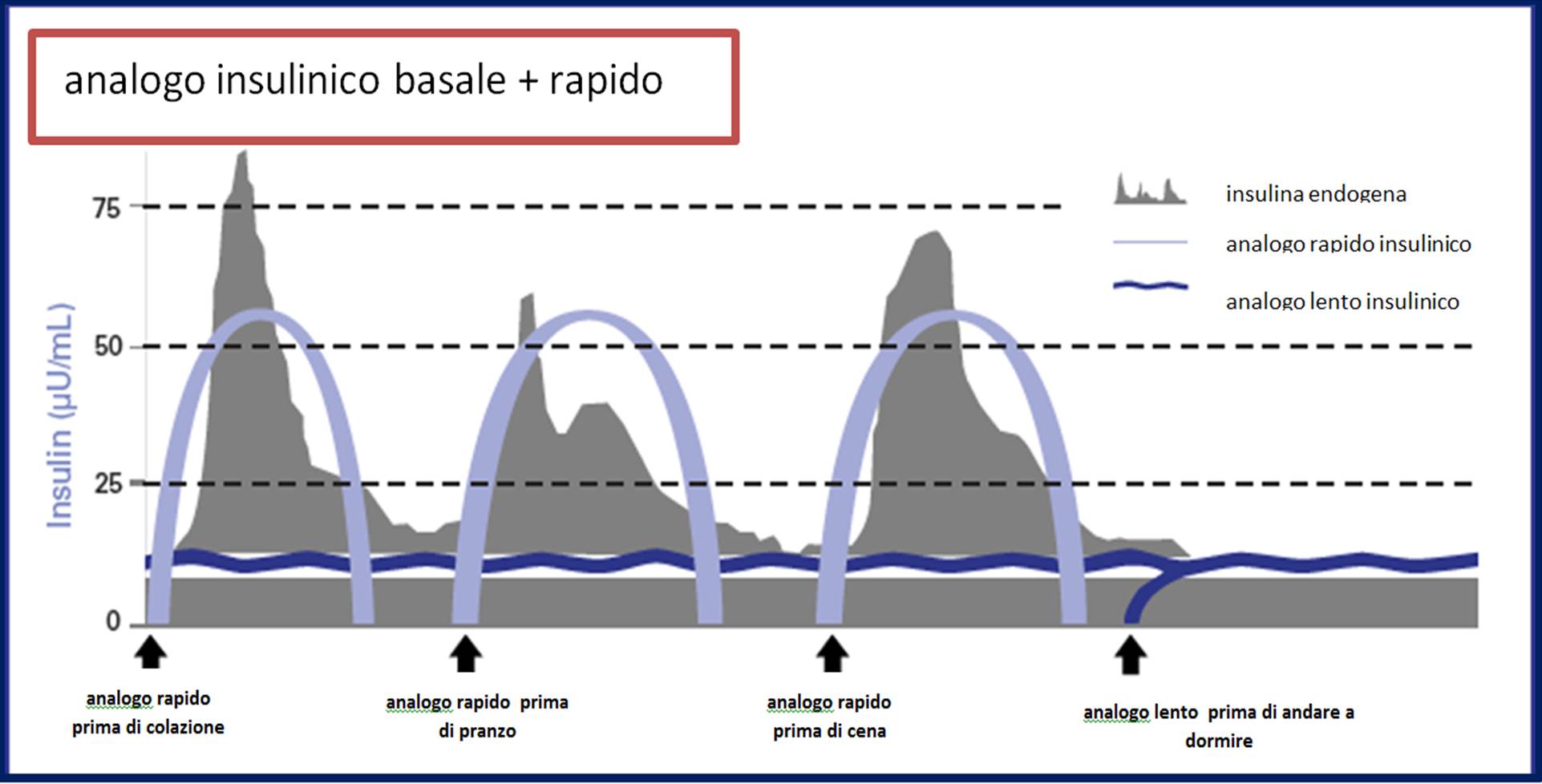
L’analogo lento imita la secrezione basale d’insulina, ossia quella quantità minima d’insulina continuamente liberata dal pancreas nelle 24 ore. L’insulina basale pone un importante freno all’attività del glucagone e degli altri ormoni controregolatori dell’insulina (cortisolo, adrenalina, ormone della crescita) sul fegato, impedendo un’eccessiva produzione di glucosio (neoglucogenesi).
Da queste considerazioni deriva che un adeguato trattamento sostitutivo insulinico deve imitare le secrezioni fisiologiche dell’insulina proprie del periodo assorbitivo (boli prandiali) e post-assorbitivo (secrezione basale), per riportare e mantenere l’equilibrio glicemico sotto controllo nei diabetici, sia prima che dopo i pasti. Ciò può essere ottenuto attraverso due modalità di somministrazione:
-lo schema multiniettivo detto basal-bolus
-il microinfusore (o pompa) d’insulina.



Leave a Reply